Razvoj lijeka je visokorizičan i dugotrajan. Čekanje na potencijalne nove tretmane teško je za pacijente, osobito one s rijetkim stanjima ili stanjima koja je teško liječiti, a ako je tržište malo, cijena odobrenog lijeka može biti visoka. Prenamjena i repozicioniranje postojećih lijekova (također poznato kao reprofiliranje) može ubrzati proces i smanjiti potrebna financijska ulaganja u usporedbi s novim lijekovima, osiguravajući da pacijenti mogu dobiti pristup liječenju brže i po pristupačnijoj cijeni.[1, 2]
Postoje četiri ključne skupine prenamijenjenih lijekova – lijekovi koji se prodaju pod postojećim ili isteklim patentima, lijekovi koji su prekinuti u kliničkim ili regulatornim fazama, stereoizomeri ili metaboliti postojećih lijekova ili kandidati kod kojih su napravljene manje promjene na postojećim lijekovima. Važno je zapamtiti da neuspjeh lijeka u kliničkim ispitivanjima nije uzrokovan samo pitanjima učinkovitosti ili sigurnosti – to može biti zato što tvrtka mijenja smjer, problemi s formulacijom ili zato što postoje problemi s komercijalnim interesom ili lošim strateškim planiranjem.[3]
Prednosti prenamjene i repozicioniranja lijekova
Iako se ova dva pojma često koriste kao sinonimi, prenamjena lijeka može se odnositi na uzimanje odobrenog lijeka i njegovu upotrebu za drugu indikaciju. Promjena položaja lijeka može se odnositi na ponovno pokretanje razvoja lijeka koji je zastao, kako bi se dobilo odobrenje za novu indikaciju.[1]
Primarne prednosti prenamjene ili repozicioniranja lijekova su trošak i vremenski aspekt. Vremenski okvir za razvoj prenamijenjenog lijeka obično je jedna do tri godine, u usporedbi s prosjekom od 12 godina za novi lijek.[4]
Za tvrtku koja razvija lijek koji je zastao u razvoju ili onaj koji je stigao na tržište za drugu indikaciju, mogućnost 'recikliranja' postojećih pretkliničkih i/ili kliničkih podataka o sigurnosti, toksičnosti i farmakokinetici/farmakodinamici uštedjet će i novac i vrijeme . Također im omogućuje da povrate novac uložen u ono što bi inače moglo biti neuspjeli lijek. Postojeće znanje također smanjuje rizik od neuspjeha.
Lijekovi koji su bili neuspješni ili neuspješni u razvoju, ali još uvijek imaju određenu patentnu zaštitu, mogu biti premješteni za drugu indikaciju od strane izvorne tvrtke ili nositelja licence. Promjena namjene također može omogućiti tvrtkama da produže životni ciklus vlastitih lijekova koji se prodaju na tržištu kojima se približava istek patenta, budući da mogu dobiti zaštitu za novu indikaciju. Promjena namjene i pozicioniranja lijekova također može biti dragocjena za tvrtke koje razvijaju lijekove za rijetke bolesti, potičući suradnju i dijeljenje podataka i resursa.[3, 5]
Koraci za razvoj i dobivanje odobrenja za prenamijenjeni lijek mogu uključivati:
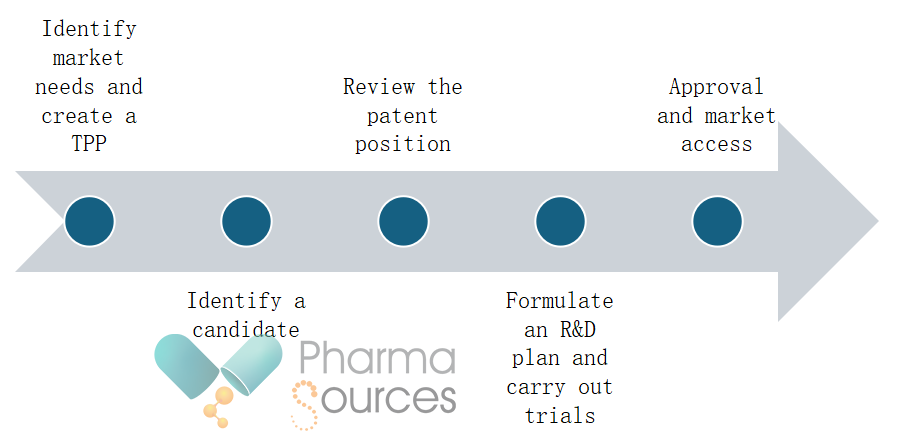
Identificirajte potrebe tržišta i izradite ciljni profil proizvoda
Za tvrtku koja želi promijeniti namjenu lijeka, ali nema postojećeg kandidata na umu, prvi korak je procijeniti tržišno okruženje kako bi se vidjelo postoji li pacijentova potreba za novim lijekom i hoće li se tvrtka moći nadoknaditi ulaganja u razvoj lijekova. To je podržano razvojem ciljanog profila proizvoda (TPP). TPP opisuje željene karakteristike lijeka u razvoju za određeni poremećaj. Tvrtki daje vodič kroz razvoj lijekova za sve uključene timove. [2, 6, 7]
Područja obuhvaćena TPP-om, koja je također korisno pregledati kada tvrtka ima na umu određenog kandidata, uključuju:[2, 7, 8]
● Indikacija
○ Početna indikacija cilja
○Moguće buduće indikacije
●Stanovništvo
○Početno ciljno tržište – ekonomski prioriteti ili područja najvećih nezadovoljenih potreba
○Izvedivost studije
○Zahtjev za popratnu dijagnostiku za identifikaciju podpopulacija
●Ciljanje/farmakokinetika
●Sigurnost, podnošljivost i učinkovitost
○ Krajnje točke studije
○Prednosti u usporedbi sa sadašnjim/budućim konkurentima ili standardom skrbi
●Interakcije lijek-lijek
● Stabilnost
○ Zahtjevi za skladištenje
○Može ovisiti o ciljnim tržištima
●Put primjene/formulacija
○Trenutna formulacija/mogućnost preformulacije
○Koji će način primjene preferirati pacijenti?
○Hoće li biti potreban uređaj za dostavu i je li već dostupan
●Učestalost doziranja
○Razmotrite u usporedbi sa standardom skrbi
● Trošak
○Ciljni trošak po dozi, na temelju analize konkurentskog okruženja
●Vrijeme do dostupnosti
○Vrijeme potrebno za klinička ispitivanja i regulatorne procese
○Vrijeme potrebno za procjene zdravstvene tehnologije (HTA)
Identificirajte kandidata
Tvrtka može imati na umu lijek kao kandidata za prenamjenu, na primjer temeljeći novu indikaciju na nalazu koji se smatra nuspojavom u prethodnom razvojnom procesu.

Za tvrtku koja traži lijek za određenu metu ili indikaciju, pristupi mogu biti ciljani, strukturni, potpisni, putni, mrežni, na znanju ili kliničkim podacima, a specifični pristupi uključuju:[13-17]
● Mendelska randomizacija za utvrđivanje odnosa između fenotipova i genetski predviđenih učinaka lijekova
● Multi-omics podataka velikih razmjera za bolje razumijevanje etiologije bolesti i identificiranje novih ciljeva lijekova
● Strojno učenje za prepoznavanje podtipova bolesti i ciljeva lijekova ili za povezivanje patologije i molekularnih mehanizama
●Generativna umjetna inteligencija ili integracija ekspresije ljudskog gena, poremećaja lijeka i kliničkih podataka, za identifikaciju kandidata
Pregledajte položaj patenta
Tvrtka koja želi promijeniti namjenu ili pozicionirati lijek mora biti svjesna postojeće patentne pozicije, uključujući patente za izvorni spoj i za formulacije, režime doziranja ili specifične upotrebe. Ako je lijek još uvijek pokriven patentom, tada će morati kontaktirati nositelja patenta i vidjeti jesu li zainteresirani za suradnju ili licenciranje lijeka. Ako lijek nije patentiran, postoji veća sloboda djelovanja.[4]
Svi lijekovi, uključujući prenamijenjene i premještene lijekove, trebaju razinu patentne zaštite kako bi se tvrtki koja prenamjenjuje omogućila da nadoknadi svoje troškove prije nego što se suoči s konkurencijom. Nove vrste patenata mogu uključivati: [4, 18]
●Terapeutska indikacija
●Formulacija
●Režim doziranja
● Sustav isporuke
● Kombinacija lijekova
●Kombinacija lijek/uređaj
Formulirajte plan istraživanja i razvoja i provedite ispitivanja
Za uspješan razvoj lijeka prenamijenjene namjene, tvrtke moraju surađivati s kliničarima i multidisciplinarnim timom unutarnjih i vanjskih stručnjaka koji podržavaju proces razvoja. Prenamijenjeni lijekovi i dalje moraju imati dovoljno pretkliničkih podataka, proći klinička ispitivanja i zadovoljiti stroge regulatorne standarde u svojoj novoj indikaciji. Iako će postojeći podaci o ljudima i ne-ljudima poduprijeti sigurnost i toksičnost, bit će potrebna daljnja klinička ispitivanja kako bi se potvrdila učinkovitost u ciljanoj skupini pacijenata prije podnošenja na odobrenje.[8]Rad s pacijentima i skupinama za zastupanje pacijenata također je važan kako bi se razumjelo što im je potrebno od liječenja i regrutirali sudionici za klinička ispitivanja.[4]
Odobrenje i pristup tržištu
Bliska suradnja s regulatornim tijelima i tijelima za procjenu zdravstvene tehnologije (HTA) podržat će učinkovit proces prema odobrenju, tržištu i nadoknadi. Regulatorna tijela mogu savjetovati koja će klinička ispitivanja biti potrebna i predložiti koji će put do odobrenja, uključujući ubrzane putove, biti najprikladniji za određeni lijek i indikaciju.[4]
Ukratko
Promjena namjene i pozicioniranja lijekova nudi isplativ i učinkovit put do tržišta koji pacijentima omogućuje brži pristup lijekovima. Tvrtke moraju biti sigurne da prikupljaju prave podatke za nesmetan proces, a tome može pomoći suradnja s pacijentima, drugim tvrtkama, regulatornim tijelima i tijelima za procjenu zdravstvene tehnologije.
Reference
1. Bakker, A., Naizgled mali semantički problem velika je prepreka razvoju liječenja rijetkih bolesti. STAT, 2023. Dostupno na: https://www.statnews.com/2023/06/27/drug-repurposing-repositioning-rare-diseases/.
2. Griffiths, A., et al., Ciljani profili proizvoda u farmaceutskom razvoju KPMG. 2023. Dostupno na: https://assets.kpmg.com/content/dam/kpmg/uk/pdf/2023/01/target-product-profiles-in-pharmaceutical-development.pdf.
3. Elvidge, S., Izvlačenje duha iz boce koji mijenja položaj lijeka. Life Science Leader, 2010. Dostupno na: https://www.lifescienceleader.com/doc/getting-the-drug-repositioning-genie-out-of-the-bottle-0001.
4. Pisani, J., et al., Promjena namjene lijekova: prilika i izazov. 2021. Dostupno na: https://www.lifearc.org/wp-content/uploads/2024/03/RD-Drug-repurposing-report.pdf.
5. Taylor, M., M. Salova i A. Schroeder, Promjena namjene lijekova: potencijal za proširenje liječenja rijetkih bolesti. Avalere: Insights & Analysis, 19. veljače 2024. Dostupno na: https://avalere.com/insights/drug-repurposing-potential-to-expand-rare-disease-treatment.
6. Staff writer. Ciljajte profile proizvoda. Svjetska zdravstvena organizacija. 9. srpnja 2024. Dostupno na: https://www.who.int/observatories/global-observatory-on-health-research-and-development/analyses-and-syntheses/target-product-profile/who-target-product -profili.
7. Pisac osoblja. Promjena namjene lijeka: ključna razmatranja. UCL Therapeutic Innovation Networks - UCL – University College London. 9. srpnja 2024. Dostupno na: https://www.ucl.ac.uk/ion/translation-enterprise/tailored-support-translational-researchers/re-purposing-drug/repurposing-drug.
8. Pisac osoblja. Repurposing Medicines Toolkit - Smjernice za navigaciju u procesu. LifeArc/Vijeće za medicinska istraživanja. 11. srpnja 2024. Dostupno na: https://www.repurposingmedicines.org.uk.
9. Okrugli stol o prevođenju genomskih istraživanja za zdravlje, Odbor za politiku zdravstvenih znanosti i Institut za medicinu, u prenamjeni i pozicioniranju lijekova: Sažetak radionice. 2014.: Washington (DC).
10. Ghofrani, HA, IH Osterloh i F. Grimminger, Sildenafil: od angine do erektilne disfunkcije do plućne hipertenzije i šire. Nat Rev Drug Discov, 2006. 5(8): str. 689-702.
11. Gohel, D., et al., Sildenafil kao lijek kandidat za Alzheimerovu bolest: Promatranje podataka o pacijentima iz stvarnog svijeta i mehanička opažanja iz pluripotentnih neurona izvedenih iz matičnih stanica izazvanih od strane pacijenata. J Alzheimers Dis, 2024. 98(2): str. 643-657.
12. Dorset Medicines Advisory Group, SMJERNICE ZA ZAJEDNIČKU NJEGU ZA SILDENAFIL ZA LIJEČENJE SEKUNDARNOG RAYNAUDSOVOG FENOMENA POVEZANOG SA SUSTAVNOM SKLEROZOM NHA. 2017. Dostupno na: https://nhsdorset.nhs.uk/Downloads/aboutus/medicines-management/Shared%20Care%20Guidelines/Sildenafil%20Shared%20Care%20Documented%20July%2017.pdf.
13. Wang, L., et al., Krajolik metodologije u prenamjeni lijekova korištenjem ljudskih genomskih podataka: sustavni pregled. Kratak Bioinform, 2024. 25(2).
14. Sperry, M. i DE Ingber, Strategije prenamjene lijekova, izazovi i uspjesi. 4. ožujka 2024. Dostupno na: https://www.technologynetworks.com/drug-discovery/articles/drug-repurposing-strategies-challenges-and-successes-384263#D3.
15. Rodriguez, S., et al., Strojno učenje identificira kandidate za prenamjenu lijekova u Alzheimerovoj bolesti. Nat Commun, 2021. 12(1): str. 1033.
16. Yan, C., et al., Iskorištavanje generativne umjetne inteligencije za davanje prioriteta kandidatima za prenamjenu lijekova za Alzheimerovu bolest uz kliničku potvrdu u stvarnom svijetu. NPJ Digit Med, 2024. 7(1): str. 46.
17. Wu, P., et al., Integriranje ekspresije gena i kliničkih podataka za identifikaciju kandidata za prenamjenu lijekova za hiperlipidemiju i hipertenziju. Nat Commun, 2022. 13(1): str. 46.
18. Conour, J., Zašto su patenti za metode liječenja prenamijenjenih lijekova vrijedni ulaganja. JD Supra: Vijesti i uvidi, 5. listopada 2020. Dostupno na: https://www.jdsupra.com/legalnews/why-method-of-treatment-patents-for-92813/.

